 |
| חיפושית הזבל. זחליה ניזונים מהפגר |
המאמר ב-PNAS
פורסם גם ב"הידען"
אוסף של כתבות ממקורות שונים שנכתבו על ידי מחברים שונים
 |
| חיפושית הזבל. זחליה ניזונים מהפגר |
מגפת השפעת הגדולה ביותר בהיסטוריה המודרנית, המכונה ״השפעת הספרדית״, התחוללה בעולם בשנים 1919-1918 וגבתה את חייהם של יותר מ-50 מיליון בני אדם, הרבה יותר מהרוגי מלחמת העולם הראשונה. אף על פי שתסמיני המחלה היו דומים לאלה שהופיעו בעת התפרצויות קודמות שלה (ובעיקר תסמינים הפוגעים בדרכי הנשימה), היה שיעור התמותה גבוה בהרבה, וחתך אוכלוסיית הנפטרים היה חריג ביותר: בעוד שפעת פוגעת קשה בתינוקות, בקשישים ובבעלי מערכת חיסון מוחלשת ואף עלולה לקטול אותם, ה״שפעת הספרדית״ הרגה גם אנשים צעירים ובריאים. התמותה נגרמה בעיקר כתוצאה מדלקת ריאות שבמהלכה התמלאו הריאות בדם או בנוזלים אחרים.
במהלך שנה אחת נפגעו אירופה, אמריקה הדרומית, אלסקה ואיים באוקיינוס השקט משלושה גלים של המגפה הקטלנית. את שמה קיבלה המגפה בשל העובדה שבספרד, שלא השתתפה במלחמת העולם הראשונה (אשר עמדה להסתיים בעת שפרצה המגפה), לא הוטלה צנזורה על פרסום דבר התפרצות המחלה, להבדיל מהמצב במדינות הלוחמות שם נשמר הדבר בסוד.
מאז ימי המגפה התקדם המחקר של נגיף השפעת באופן משמעותי ביותר. בזמן המגפה טרם ידעו כיצד לבודד את נגיף השפעת. למעשה, נגיף השפעת הראשון בודד וגודל בתרבית רק בשנת 1933.
נגיפי השפעת הם נגיפי RNA חד-גדילי העטופים במעטפת ליפידית. הם החברים העיקריים במשפחת ה- Orthomyxoviridae ונחלקים לשלושה זנים: B ,A ו-C על-פי ההבדלים בחלבונים הפנימיים, בארגון הגנום, בפתוגניות ובטווח המאכסנים. הגנום הנגיפי מורכב מ-8 מקטעים, המקודדים יצירת חלבונים שונים ובהם המאגלוטינין (HA) ונוראמינידז (NA). מולקולות ההמאגלוטינין משמשות את הנגיף לשם קישור לקולטנים על פני תאים מסוימים של המאכסן (תאים במערכת הנשימה אצל יונקים), ואילו החלבון נוראמינידז מאפשר לשחרר עותקים חדשים של הנגיף מתוך התאים החופשיים ולהדביק תאים נוספים.
חלבונים אלה יוצרים בליטות (Spikes) עלי גבי השטח החיצוני של הנגיף ולהם חשיבות רבה בתגובה החיסונית של הגוף משום שהנוגדנים פועלים נגדם. נגיף השפעת מזן A מסווג לתת-זנים על-פי סוגי ה-HA וה-NA, וכיום מוכרים 16 סוגי HA ו-9 סוגי NA.
בשנת 2005 פרסמו ג׳פרי טאובנברגר (Taubenberger) ועמיתיו מהמכון לפתולוגיה של הצבא האמריקאי בוושינגטון בכתב העת המדעי Nature, שהצליחו לבודד לראשונה את הנגיף הספציפי של ה״שפעת הספרדית״ מגופות של קורבנות המגפה ולהפיק ממנו RNA.
באמצעות פענוח הרצפים הגנטיים של הנגיף הקטלני נמצא כי החלבון HA של נגיף ה״שפעת הספרדית״ היה דומה מאד לחלבון HA של נגיף שפעת העופות, וסווג כ"H1N1" (סיווג הנגיפים נעשה על-פי סוג חלבון ה-HA וחלבון ה-NA, אשר תוארו לעיל). ניסויים בנגיפים מהונדסים, המכילים את הגנים של הנגיף הקטלני, הצביעו על האפשרות שהנגיף מסוגל להפעיל את מערכת החיסון וליצור תגובה חיסונית חזקה מדי והרסנית למאכסן. ככל הנראה דיכא הנגיף את התגובה הטבעית (הנכונה) כנגד נגיפים - כגון שחרור אינטרפרון - ובמקום זאת יצר "סערת ציטוקינים" שגרמה להפעלת יתר של מערכת החיסון, תגובה שמזכירה אלרגיה או אולי אפילו מחלה אוטואימונית.
לאחר חשיפה ראשונה לשפעת מערכת החיסון של המאכסן מייצרת בדרך כלל נוגדנים כנגד חלבוני HA ו-NA של הנגיף, וכך נמנעת הדבקה חוזרת באותו נגיף. אולם, הנגיף נוטה לעבור שינויים רבים וליצור שילובים חדשים של שני החלבונים הללו. נוצר איזון עדין בין יכולתו של הנגיף להשתנות באופן שלא יוכר על ידי מערכת החיסון של המאכסן ליכולתו לעבור בקלות ממאכסן אחד למשנהו, איזון הקובע את רמת הסכנה הטמונה בנגיף.
צילום במקרוסקופ אלקטרונים סורק של נגיף השפעת הספרדית. צולם ב-2005 - לאחר גידול הנגיף בתרבית תאים. CDC/Cynthia Goldsmith |
בחודש אוגוסט השנה התפרסם ב-Nature מחקר חדש, המצביע על התפתחות מעניינת ומפתיעה בחקר הנגיף הקטלני. בראש המחקר עמדו ג׳יימס קראו (Crowe) ממכון המחקר סקריפס בקליפורניה, כריסטופר באסלר (Basler) מבית הספר לרפואה "הר סיני" בניו יורק ואריק אלטשולר (Altschuler) מביה״ס לרפואה בניו-ג׳רסי.
החוקרים אספו דגימות דם מ-32 קשישים בגילאים 101-91, כלומר מי שהיו ילדים בעת המגפה. רבים מהם יכלו לזכור קרוב משפחה חולה בסביבתם הקרובה, ולפיכך היה סיכוי כי הם עצמם היו חשופים לנגיף. בדמם של כל הקשישים שנבדקו נמצא כייל גבוה של נוגדנים נגד נגיף המגפה "הספרדית״. ממצא זה היה מפתיע, הן משום שעברו 90 שנה מאז המגפה והן משום שמדובר באנשים קשישים מאד וצפוי היה שמערכת החיסון שלהם תהיה מוחלשת. לשם השוואה בדקו החוקרים גם דגימות דם מילידי השנים שלאחר המגפה, ובדמם נמצא כייל נוגדנים נמוך בהרבה כנגד נגיף זה.
החוקרים בודדו תאי B - התאים האחראיים על ייצור הנוגדנים - מדגימות הדם שנלקחו מהקשישים. התאים גודלו בתרביות וייצרו נוגדנים לנגיף. בהמשך איחו החוקרים את תאי B הללו עם תאי מיאלומה, תאי B סרטניים, על מנת ליצור "שורת תאים" המייצרת באופן קבוע נוגדנים חד-שבטיים (כלומר, נוגדנים זהים, המכוונים כולם כלפי אותו אתר מטרה בנגיף) לנגיף השפעת ה״ספרדית". יעילות הנוגדנים המופרשים נבדקה על זנים שונים של נגיפי שפעת ונמצא כי הנוגדנים הללו מגיבים תגובה חזקה דווקא כנגד הנגיף של המגפה מ-1918 וכנגד נגיף שפעת חזירים מ־1930, אך אינם מגיבים כך לזנים נוספים של נגיף השפעת.
כדי לבדוק את פעילות הנוגדנים הללו בתוך הגוף הדביקו החוקרים עכברים בנגיף השפעת מ־1918 , ולאחר יום קיבלו העכברים נוגדנים במינונים שונים. העכברים שקיבלו מינון מספק של הנוגדנים שרדו ואילו אלה שקיבלו את נוגדן הביקורת מתו עכברים שקיבלו מינונים נמוכים יותר של הנוגדנים מתו בסופו של דבר, אך בכל זאת שרדו תקופה ארוכה יותר מאשר העכברים שקיבלו את נוגדן הביקורת.
ממצאים אלה מצביעים על כך שגם תשעה עשורים לאחר המגפה, תאי B במערכת החיסון שלנו אינם שוכחים נגיפים מסוימים וממשיכים לייצר נוגדנים ולהתכונן להתפרצות הבאה. הכושר לייצר נוגדנים אלה נשמר והנוגדנים עברו שינויים אקראיים שעשויים להגדיל את הסיכוי כי יזהו נגיפים שעברו שינויים אקראיים (מוטציות קלות ב-HA או ב-NA).
הנוגדנים המופקים במעבדה עשויים לשמש לטיפול במקרה של התפרצות חוזרת של נגיף הדומה לנגיף מ-1918 וכן עשויים לסייע בהבנת הביולוגיה של הנגיף הקטלני, שכן טרם פוענח המנגנון הגורם לו להיותו כה קטלני.
עם זאת, יש לזכור כי לא ברור האם הקשישים שהנוגדנים זוהו בדמם הם הכלל או היוצא מן הכלל: ייתכן שיש קשר בין העובדה שקשישים אלו נדבקו ושרדו את המגפה ובין הימצאות הנוגדנים בגופם בטווח זמן כה ארוך, ולכן אולי לא ניתן להסיק ממקרים אלו לגבי מנגנון ה״זיכרון החיסוני" בכלל האוכלוסייה.
כמו כן אין וודאות כי מקורם של הנוגדנים שבודדו אכן במגפת 1918. היעילות הגבוהה של הנוגדנים כנגד הנגיף וההיסטוריה של הקשישים הם שייחסו את הנוגדנים למגפה, וסביר להניח כי נגיפים דומים נוספים שבהם הודבקו הקשישים במהלך חייהם תרמו ליכולת המערכות החיסוניות שלהם לשמר אותם תאי B.
פורסם ב"גליליאו" 122, אוקטובר 2008
 |
| צבר של חיידקי E. coli Eric Erbe, digital colorization by Christopher Pooley, both of USDA, ARS, EMU |
 |
| המקור - Yale Rosen, Flicker |
 |
פצעי הרפס על השפתיים
המקור: CDC/ Dr. Herrmann
|
 |
פצעי הרפס על הלשון
המקור: CDC/ Robert E. Sumpter
|
 |
| שלבקת חוגרת על זרוע של ילד צילום: James Heilman, MD, wikimedia commons |
הנגיף המסתתר
פרופ׳ ישראל שטיינר, אתה חוקר ורופא מומחה למחלות שגורמים נגיפי ההרפס. מהי שכיחות הנשאים של HSV1 וHSV2- באוכלוסייה?
HSV1 נפוץ מאוד, 95%-90% מהאוכלוסייה נושאים אותו. לעומת זאת, לגבי HSV2 התמונה פחות חד-משמעית. והמספרים משתנים בהתאם לחברה שבה מדובר. בארץ אחוזי הנשאים של HSV2 נמוכים יחסית, 40%-20%. בצפון אמריקה מדובר במספרים גבוהים יותר. 60% ויותר.
מבחינה אפידמיולוגיה, בשנות התשעים היתה עלייה בתחלואה כתוצאה מ־HSV2. עליה זו נבלמה בשנות האלפיים. לעומת זאת, אין שינויים משמעותיים בתחלואה כתוצאה מ־HSV1 לאורך השנים.
הנגיפים HSV2-1 HSV1 שייכים לאותה המשפחה, ויש ביניהם דמיון רב. האם נשאות של נגיף מסוג HSV1 מהווה חיסון בפני הדבקה ב-HSV2, ולהפך?
אמנם יש דמיון בנוגדנים המתפתחים בגוף כנגד שני סוגי הנגיפים. אך הדבקה בסוג האחד אינה מחסנת בפני הסוג האחר, ובהחלט ישנם אנשים המודבקים בשני סוגי הנגיף. כלומר, אדם שסיכל מהתפרצויות של הנגיף באזור השפה. איננו חסין מפני הדבקה באיברי המין. ולהפך.
האם חשיפה לנגיף יכולה לגרום להתפרצות או להוות סכנה כלשהי לאדם שכבר נושא את הנגיף?
לא. לאדם שכבר נושא בגופו את הנגיף אין נשקפת סכנה בעקבות חשיפה נוספת. בדרך-כלל ההדבקה מתרחשת כאשר אדם שאינו נושא את הנגיף בא במגע עם אדם הסובל מהתפרצות מחודשת של הנגיף.
האם גירויים מכניים, כגון טיפול קוסמטי, עלולים לגרום להתפרצות מחודשת של הנגיף?
בהחלט, ידועים מקרים של ניתוחי פנים, טיפולי שיניים וניתוחים נוירוכירורגיים שגרמו להתפרצות מחודשת.
מהם, לדעתך, אמצעי הזהירות שיש לנקוט בלידה כאשר האם נושאת את נגיף ההרפס מסוג HSV2?
זוהי שאלה פתוחה, שאין עליה תשובה חד-משמעית. נגיף ההרפס עלול לגרום נזק קשה ליילוד, ולפיכך המלצתי היא על ניתוח קיסרי בכל מקרה של התפרצות שלפוחיות הרפס באיברי המין בעברה של היולדת (כלומר, אפילו כאשר לא היו התפרצויות בסמוך ללידה או במהלך ההיריון).
מחקרים רבים עסקו לאחרונה ביכולת של נגיפי ה־HSV להיכנס למצב רדום, ואף פוענח המנגנון המאפשר את הקיום הלטנטי של הנגיף. האם לטנטיות זו של נגיפי ה-HSV שונה במהותה מזו הקיימת בנגיפים אחרים?
בהחלט קיימים הבדלים רבים. נגיף אחר ממשפחת ההרפס, Varicella zoster הגורם לאבעבועות רוח בילדות ולמחלת השלבקת החוגרת אם הוא מתפרץ שוב לאחר שנים, נשאר אף הוא רדום בגופנו. ואולם, בעוד HSV גורם למחלה מצומצמת יותר וההתפרצויות הן בתדירות גבוהה יחסית (פעם בחודש עד פעם בשנים אחדות), השלבקת החוגרת מתפרצת בדרך כלל באנשים קשישים וההתפרצויות הן נדירות מאוד, בדרך־כלל פעם או פעמיים בלבד במהלך החיים.
מבחינת המנגנון המאפשר את הכניסה למצב רדום ב-HSV התברר שמעורב בו ה-microRNA של הגן LAT, ואילו לגבי Varicella zoster טרם פוענח המנגנון המאפשר את המצב הלטנטי.
במחקרים שונים מוזכר HIV כנגיף המסוגל להיכנס למצב רדום. אך למעשה נגיף זה איננו מתאים להגדרה הקלאסית של ״נגיף לטנטי״, משום שהוא מקיים מחזור רבייה מלא, אלא שקצב ההתרבות הוא אטי.
האם תופעת הלטנטיות מעידה על כשל חיסוני?
ביחס להרפס סימפלקס, מערכת החיסון אינה יעילה כנגד הנגיף, משום שהנגיף אינו יוצא מתוך התא המודבק (הנגיף נודד לאורך האקסון של תא העצב עד מקום ההתפרצות בעור. ואינו חשוף למערכת החיסון). התפרצות מחודשת של הרפס סימפלקס אינה מהווה כשל חיסוני. למעט המקרה של מושתלי מח עצם, הסובלים מהתפרצויות חוזרות של הנגיף בתדירות גבוהה יותר מאשר באנשים בריאים, בשל חולשת מערכת החיסון שלהם. לעומת זאת הנגיף Varicella zoster מתפרץ מחדש בדרך-כלל באנשים קשישים הסובלים מדיכוי טבעי (הנגרם עם הגיל) של המערכת החיסונית.
האם התרופה אציקלוויר, שפותחה נגד נגיף ההרפס, מהווה פתרון של ממש לסובלים מהנגיף?
האציקלוויר משמשת לטיפול הן בהרפס סימפלקס (HSV1 ו-HSV2) והן בשלבקת חוגרת. למעשה, התרופה יעילה יותר בטיפול בשלבקת חוגרת וזאת משום שנגיפי Varicella zoster יוצאים מתוך התא ולפיכך חשופים יותר לתרופה, ולעומתם נגיפי הסימפלקס, כאמור, אינם יוצאים מתוך תא העצב ולפיכך חשופים פחות לתרופה.
בהקשר זה ראוי להזכיר כי לאחרונה טיפלנו בבית-החולים הדסה בהר הצופים בחולה שלקתה באנצפליטיס (דלקת המוח), שבמקרים נדירים נגרמת על־יד׳ נגיף ההרפס. חולה זו לא סבלה בעבר מהתפרצויות של הנגיף. אף על פי כן, האבחנה שלנו היתה מיידית, והחולה החלימה לחלוטין. הטיפול היה מתן אציקלוויר דרך הווריד.
מדוע אין חיסון נגד הרפס? האם חיסון כזה נמצא בשלבי פיתוח?
ישנו חיסון כנגד הנגיף Varicella zoster, הניתן בדרך־כלל נגד אבעבועות רוח, אך הוא יעיל גם נגד שלבקת חוגרת במדוכאי חיסון וניתן בדרך-כלל לקשישים. אין כיום חיסון כנגד הרפס סימפלקס, כיוון שחיסון זה לא ימנע מהנגיף להסתתר ולהימצא באופן רדום בתוך תאים. מנסים לפתח חיסון שיפעל גם כשהנגיף נמצא בתוך התאים, אך הדרך עוד ארוכה, כיוון שכך, הדבקה לטנטית הנגיף מוסתר למעשה ממערכת החיסון. בינתיים אין פריצות דרך שיובילו לפיתוח חיסון או טיפול יעיל יותר מהקיים.
האם יש קשר בין נגיף ההרפס סימפלקס למחלת הסרטן?
אין עדויות לקשר של הרפס סימפלקס לסרטן. בסוגי הרפס אחרים ישנו קשר מובהק. למשל בנגיף אפשטיין־בר וכמובן בסרקומת קפושי, שגורם HSV8, נגיף ממשפחת ההרפס.
כיצד יכול נגיף ההרפס לגרום לדלקת המוח (אנצפליטיס)?
באופן תיאורטי, ישנם כמה מגנונים אפשריים. כתוצאה מזיהום ראשוני, שפעול מחדש מתוך הגנגליונים התחושתיים, או שפעול מתוך רקמת המוח. דלקת המוח מסוכנת במיוחד בילדים. אך לא ברור עדיין מה גורם למקרים שבהם הרפס מוביל לדלקת המוח. לאחרונה התפרסם מחקר שלפיו ילדים שפיתחו דלקת מוח כתוצאה מהרפס לוקים בפגם גנטי.
פרופ' ישראל שטיינר הוא רופא ראשי מומחה בנוירולוגיה בבית-החולים הדסה בירושלים. המתמחה בין היתר במחלות שגורמים נגיפי ההרפס וחוקר זיהומים לטנטיים בנגיפי הרפס במערכת העצבים.
|
 |
| תמונת מיקרוסקופ אלקטרוני: ביופילם של Pseudomonas aeruginosa שהתפתח על גבי קתטר |
 |
| משמאל לימין: קישור הפיך לפני השטח; היצמדות חזקה יותר ובלתי הפיכה; הפרשת חומר חוץ-תאי פולימרי והבשלת הביופילם; שחרור תאים מהקרום |
 |
| תמונת מיקרוסקופ אלקטרונים של נגיפי פפילומה של האדם (הצבעים הוספו לתמונה לשם הדגשה) |
 |
| תרשים של איברי הרבייה של האשה |
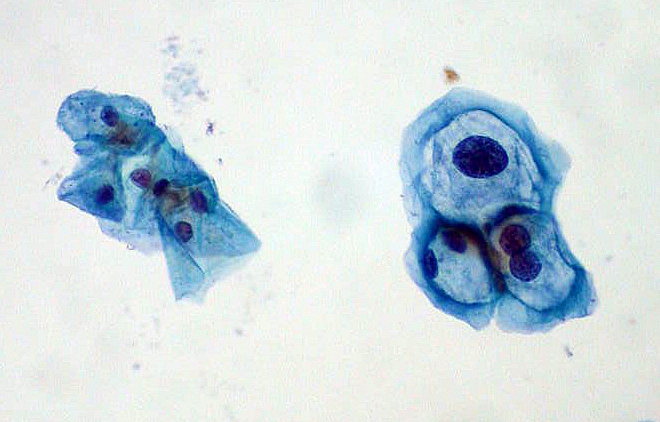 |
| תאים מבדיקת פאפ - לאבחון גידולים בצוואר הרחם. משמאל תאים תקינים, מימין תאים מודבקים בנגיפי פפילומה. המקור: Ed Uthman, Flicker |